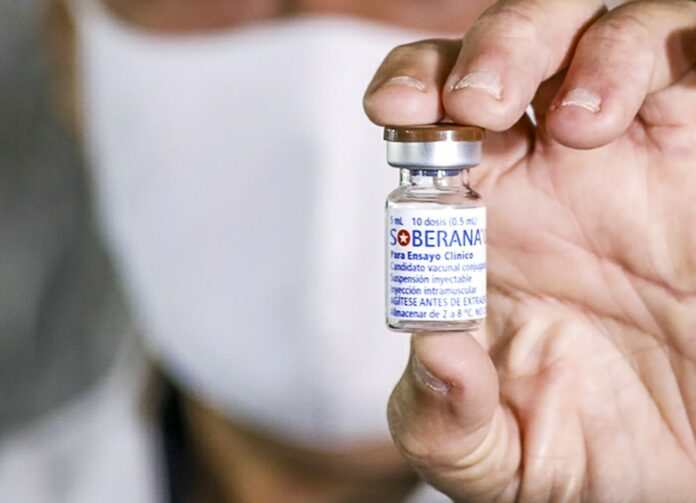
Foto: Roy Leyra
Texto: Mónica Fernández
La televisión estatal de Irán ha reportado que el país ha concedido el uso de emergencia de su primera vacuna contra el COVID-19, denominada COVIran Barekat, debido a la escasa disponibilidad de otras opciones. El ministro de Salud de Irán declaró: «Pasteur, que es una de las mejores vacunas gracias a la colaboración tecnológica entre nuestro país y Cuba, recibirá el permiso para su uso de emergencia a principios de la próxima semana».
¿Y cómo surgió el nombre Pasteur? Este nombre fue elegido para el candidato vacunal Soberana 02 en Irán, en homenaje al centro donde se está elaborando la vacuna.
El 8 de enero de 2021, el Instituto Finlay de Vacunas de Cuba y el Instituto Pasteur de Irán firmaron un acuerdo para llevar a cabo un ensayo clínico de fase III del candidato vacunal Soberana 02. La prensa cubana informó sobre dos razones para este convenio: la necesidad de evaluar el rendimiento de la vacuna en diferentes contextos con variadas incidencias de la enfermedad, y la urgencia de aumentar la capacidad de producción para inmunizar a la población cubana.
El vocero del comité iraní de combate a la COVID-19, Kianush Yahanpur, indicó que la condición para realizar el ensayo clínico en su población fue que existiera «una producción conjunta de la vacuna y una transferencia de tecnología» al país persa. El acuerdo finalmente firmado incluyó el envío de 100,000 dosis de Soberana 02 (las cuales arribaron a Irán el 11 de marzo), así como la transferencia de tecnología para su eventual producción nacional.
En abril, comenzó el ensayo con 24,000 voluntarios, y el director del Instituto Pasteur, Alireza Biglari, comentó: «Al administrar dos dosis, la vacuna (Soberana) mostró una eficacia superior al 80% y era la única vacuna para la que también se diseñó una dosis de refuerzo. Al usar la dosis de refuerzo, podemos afirmar con orgullo que tiene una efectividad del 100%».
La prensa estatal iraní informó que, como parte del acuerdo, tras la vacunación de 50,000 iraníes durante la fase III del ensayo, la vacuna estaría disponible al público en junio, con dos millones de dosis, lo cual se concretará la próxima semana al recibir la autorización para su uso masivo.